I processi biologici che determinano l'healthspan Parte II
Analisi dei percorsi molecolari e metabolici
Nota dell’autore
In questa seconda parte entriamo nel cuore della biologia del declino: i 12 hallmarks che determinano la qualità della salute nel tempo. Alcune sezioni possono risultare più tecniche delle precedenti , ma ho cercato di renderle accessibili senza perdere precisione scientifica. L’obiettivo è offrirti alcuni punti chiave per orientarti tra i processi biologici che influenzano l’healthspan. Se qualcosa non è chiaro o vuoi approfondire un punto, puoi scriverlo nei commenti: risponderò con piacere.
Buona lettura.
Dott. Letizia Foglieni – Medico Chirurgo
Capita spesso di avvertire che qualcosa cambia: l’energia non è più la stessa, il recupero richiede più tempo. Non si tratta solo di stili di vita, dipende da ciò che avviene all’interno delle cellule, nei sistemi che regolano l’energia, la riparazione e le risposte allo stress.
La prima parte dell’articolo ha introdotto il concetto di durata della salute (healthspan) come metrica per comprendere la qualità di vita; in questa seconda parte si analizzano, senza entrare in tecnicismi, i percorsi molecolari e metabolici che compromettono la funzionalità nel tempo.
Decodificare tali meccanismi permette di cogliere i motivi per cui alcune persone mantengono autonomia e vitalità più a lungo.
Perché i processi biologici determinano l’healthspan
Si entra ora nel vivo dell’analisi dei principali sistemi biologici coinvolti: dai meccanismi di riparazione del danno alla gestione dell’energia cellulare e delle risposte allo stress, processi che nel tempo influenzano il benessere individuale nel tempo.
La prospettiva della geroscienza
La geroscienza studia le variazioni della salute non come fenomeni a se stanti, ma analizza una rete interconnessa di processi biologici che creano un circolo vizioso del decadimento funzionale.
Ricercatori come López‑Otín e Blasco hanno dimostrato come i sistemi deputati alla gestione di danno cellulare, energia e stress siano direttamente collegati e in grado di mantenere l’equilibrio funzionale. Nel momento in cui uno si altera gli effetti si propagano agli altri con una reazione a catena che spiega la diversità dei percorsi di invecchiamento individuale.
I segni distintivi come mappa dei processi biologici
La scienza moderna interpreta il passare degli anni non come un declino casuale, ma come un processo caratterizzato da 12 “segni distintivi” (hallmarks) che, nel loro insieme, danno origine ad una mappa biologica di eventi interconnessi che agiscono simultaneamente sul deterioramento cellulare.
Questi hallmarks comprendono sia disfunzioni sistemiche come l’infiammazione cronica e la disbiosi, sia danni molecolari come l’accorciamento dei telomeri e l’instabilità genomica.
Per semplice informazione descrittiva, per la maggior parte della ricerca, i 12 hallmark vengono suddivisi in tre categorie: “primari”, “antagonisti” e “integrativi”.
I tratti distintivi “primari” descrivono soprattutto forme di danno molecolare e perdita dei sistemi di controllo della qualità cellulare che, accumulandosi, innescano risposte compensative e riorganizzazioni cellulari che nel tempo possono diventare disfunzionali.
I principali sono:
instabilità genomica
accorciamento dei telomeri
alterazioni epigenetiche
perdita di proteostasi
autofagia disfunzionale.
I tratti distintivi “antagonistici” descrivono risposte cellulari nate come adattative (ad esempio a nutrienti o stress) che, quando cronicizzano o si deregolano diventano promotrici e pro-invecchiamento, influenzando più tessuti e funzioni.
I principali sono:
deregolazione del rilevamento dei nutrienti (nutrient sensing)
disfunzione mitocondriale
senescenza cellulare
I tratti distintivi “integrativi” rappresentano livelli in cui disfunzioni cellulari e segnali tissutali convergono nella perdita di funzione multi-organo, avvicinandosi al concetto operativo di salute come capacità di mantenere omeostasi e rispondere in modo efficace allo stress.
I principali sono:
esaurimento delle cellule staminali
comunicazione intercellulare alterata
infiammazione cronica
disbiosi.
Danno e riparazione: DNA, epigenetica e qualità delle proteine (proteostasi)
In questa categoria troviamo i principali “colpevoli”, gli hallmark primari: processi che generano il danno molecolare iniziale e danno origine alla senescenza biologica.
Instabilità genomica
E’ il fattore più evidente. Con il trascorrere del tempo aumentano le mutazioni, le rotture del DNA, il nostro “libretto delle istruzioni”, e i sistemi di riparazione hanno difficoltà ad arginare il danno, compromettendo la capacità della cellula di mantenere in equilibrio tutti i meccanismi interni.
L’ accumulo di danni contribuisce al così detto stress replicativo: la cellula non é più in grado di duplicare in maniera corretta il proprio DNA per creare nuove cellule, come una fotocopiatrice che, con l’usura, fornisce copie sempre più sbiadite e illeggibili.
Accorciamento dei telomeri
A tutto ciò si aggiunge la progressiva riduzione di queste strutture protettive (telomeri) che determina a sua volta un arresto del ciclo cellulare permanente, seguito da senescenza e morte delle cellule.
Alcuni ricercatori hanno dimostrato che anche una singola esposizione a uno stress ossidativo, mirato ai telomeri, è sufficiente ad inibire la crescita cellulare e in grado di indurre senescenza prematura come evidenziato da Barnes et al. (2022) e confermato da studi successivi.
Alterazioni epigenetiche
Tali alterazioni si manifestano sia come modifiche nei sistemi che controllano l’organizzazione del DNA, sia come segnali misurabili dagli orologi epigenetici: formule matematiche che calcolano l’età biologica analizzando come variano nel tempo alcuni fenomeni chimici, in particolare la metilazione.
È importante distinguere tra età cronologica ed età biologica: mentre la prima indica semplicemente gli anni trascorsi dalla nascita, la seconda riflette lo stato di salute del nostro organismo.
Grazie agli orologi epigenetici, oggi é possibile stabilire come due persone con egual età anagrafica abbiano differente età biologica definita dal loro stile di vita e dalle esposizioni ambientali. A solo scopo informativo, i più conosciuti orologi epigenetici sono: l’orologio di Horvath e l’orologio di GrimAge che analizzano i livelli di metilazione del DNA e quanto la velocità del declino cellulare si discosti dalla media.
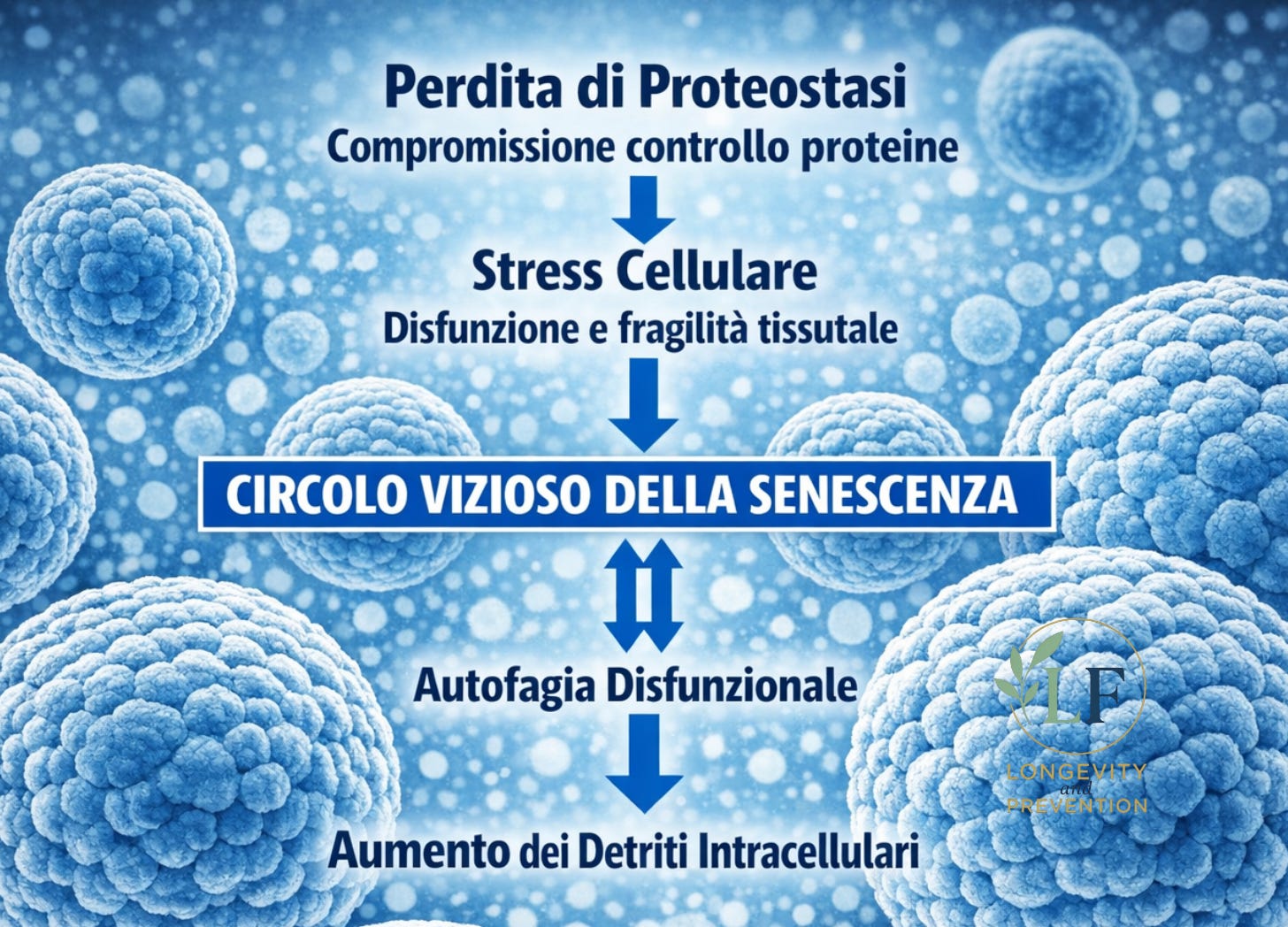
Perdita di proteostasi
La proteostasi è un sistema che permette di mantenere la qualità, la produzione e lo smaltimento corretti delle proteine che costituiscono i “mattoni” fondamentali dei tessuti.
Con il trascorrere dell’età questi meccanismi perdono efficienza: le proteine si accumulano, e secondo Skowronska‑Krawczyk, concorrono alla fragilità tissutale e all’innesco di numerose patologie croniche tra cui neurodegenerazioni e infiammazione cronica.
Autofagia disfunzionale
L’autofagia è un meccanismo essenziale per mantenere la cellula in condizioni sane. Le strutture danneggiate e in eccesso vengono degradate e smaltite in una vera e propria “pulizia interna” che, se viene meno, determina accumulo di detriti intracellulari, i quali contribuiscono al deficit della proteostasi e alla fragilità di tessuti e organi.
L’autofagia disfunzionale non è solo una conseguenza del trascorrere dell’età, ma anche uno dei meccanismi che ne accelerano gli effetti negativi sull’organismo.
Energia e metabolismo: mitocondri, NAD⁺ e nutrient sensing
Il metabolismo energetico è uno dei pilastri fondamentali della salute cellulare: garantisce la produzione di energia, regola l’equilibrio tra sintesi, riparazione e degradazione e risponde in maniera dinamica alla disponibilità di nutrienti.
Quando questi meccanismi perdono efficienza, le risposte nate per proteggere la cellula, si trasformano in promotrici del danno, ed è qui che entrano in gioco i “tratti antagonistici”.
Mitocondri
I mitocondri sono molto più di semplici produttori di energia: sono organelli dinamici che regolano il metabolismo cellulare, gestiscono lo stress ossidativo e partecipano attivamente alle decisioni sul destino della cellula. È una visione ormai consolidata, ribadita anche da López‑Otín et al. (2022), che includono la disfunzione mitocondriale tra i tratti chiave che guidano il declino funzionale dei tessuti.
Il declino mitocondriale si manifesta con una ridotta capacità di produrre energia e un aumento della produzione di specie reattive dell’ossigeno, i cosiddetti ROS, che accumulandosi, oltre la soglia neutralizzabile dalla cellula, danneggiano proteine, lipidi e DNA, innescando un circolo che si autoalimenta.
Vizioli et al. (2020) hanno inoltre dimostrato che i mitocondri disfunzionali inviano segnali al nucleo della cellula, contribuendo all’attivazione di risposte infiammatorie: un ponte diretto tra inefficienza energetica e fragilità tissutale.
A complicare il quadro si aggiunge il declino della mitofagia, il processo con cui la cellula elimina i mitocondri danneggiati.
Quando questo meccanismo di sorveglianza si indebolisce, i mitocondri compromessi si accumulano, amplificando lo stress ossidativo e rendendo la cellula sempre più vulnerabile.
NAD⁺ (Nicotinamide adenina dinucleotide)
E’ una molecola molto versatile e indispensabile per la produzione d’energia, la riparazione del DNA, la regolazione dell’infiammazione e l’attività di enzimi chiave come le sirtuine.
Con il trascorrere degli anni, i livelli diminuiscono progressivamente. McReynolds et al. (2020) dimostrano come questo calo comprometta sia la funzione mitocondriale sia i meccanismi di difesa, riducendo l’attività delle sirtuine e creando un circolo che si autoalimenta.
E’ affascinante come una molecola così piccola riesca a orchestrare processi tanto diversi: energia, riparazione, resilienza. Per questo motivo, molte ricerche si concentrano su strategie per ripristinare i livelli fisiologici per mantenere la funzionalità cellulare.
Deregolazione del rilevamento dei nutrienti (nutrient sensing)
Le cellule non sono solo spettatrici di ciò che mangiamo, ma possiedono veri e propri “sensori” per monitorare costantemente la disponibilità di energia e nutrienti.
Questo sistema è governato da un gioco di equilibri tra due sensori con funzioni opposte: mTOR, che rileva l’abbondanza e promuove la crescita e la costruzione di proteine, e AMPK, che rileva la scarsità e attiva programmi di risparmio, riparazione e smaltimento dei componenti danneggiati.
Nel corso del tempo, questo raffinato meccanismo si altera: le cellule possono trovarsi in uno stato di “abbondanza perenne” (eccesso di segnale mTOR), che impedisce la pulizia interna tramite il meccanismo dell’autofagia e favorisce l’insulino-resistenza.
È anche per questo che molti interventi per promuovere la longevità, come la restrizione calorica o l’uso di alcuni farmaci tra cui la metformina, mirano proprio ad “ingannare” questi sensori per riportare la cellula in una modalità di riparazione e mantenimento.
Senescenza e infiammazione: SASP, immunosenescenza e inflammaging
La perdita della capacità di mantenere equilibrio e funzionalità cellulare, dipende da meccanismi che riconoscono il danno e lo gestiscono.
Alcuni appartengono ai tratti antagonistici, come la senescenza cellulare, altri ai tratti integrativi, come l’immunosenescenza e l‘inflammaging.
Tra questi due livelli si colloca il SASP: nato come risposta protettiva, può diventare il ponte che trasforma una difesa locale in infiammazione sistemica.
Senescenza cellulare
Si tratta di uno stato di arresto della crescita che le cellule adottano in risposta a vari stress, come l’accorciamento dei telomeri, il danno al DNA o stimoli proliferativi anomali, come nel caso delle cellule tumorali.
Per questo motivo, la senescenza è classificata come un hallmark antagonistico: nasce per proteggere, blocca la proliferazione delle cellule danneggiate e segnala al sistema immunitario quali cellule degradate sono da eliminare.
L’equilibrio si altera quando le cellule senescenti si accumulano più rapidamente di quanto possano essere rimosse: la cellula non prolifera più, ma rimane metabolicamente attiva, spesso descritta come “cellula zombie”, e inizia a influenzare negativamente il tessuto circostante.
È qui che entra in scena SASP, che rappresenta il ponte naturale verso i tratti integrativi.
SASP (Senescence-Associated Secretory Phenotype)
E’ un meccanismo protettivo identificato da Campisi nei primi anni 2000 e approfondito da López-Otín et al. nel 2013, attraverso cui le cellule senescenti secernono un cocktail di molecole infiammatorie, tra cui citochine, proteasi e fattori di crescita che alterano l’ambiente cellulare.
In condizioni normali, grazie all’intervento del sistema immunitario, la cellula danneggiata viene eliminata, mentre quando le cellule senescenti si accumulano più rapidamente di quanto il sistema immunitario riesca a eliminarle, il SASP diventa una fonte cronica di infiammazione perdendo la funzione protettiva.
Immunosenescenza
E’ considerata un tratto integrativo: non è un processo isolato, ma la conseguenza sistemica dell’interazione prolungata tra senescenza, infiammazione e perdita di efficienza dei meccanismi di controllo.
Con il passare degli anni, la funzionalità del sistema immunitario subisce un progressivo declino: perde la capacità di rispondere efficacemente alle infezioni e diminuisce la facoltà di distinguere ciò che è innocuo da ciò che è pericoloso.
Il fenomeno è stato inquadrato da López-Otín et al. (2022) tra i meccanismi che collegano senescenza cellulare e infiammazione cronica. Nel 2023 Li et al. dimostravano come l’infiammazione cronica acceleri a sua volta il declino delle cellule immunitarie, rendendo sempre più difficile eliminare le cellule senescenti e i fattori infiammatori che rilasciano.
Una delle conseguenze più visibili nella vita quotidiana è la minore efficacia dei vaccini negli adulti più avanti negli anni: le risposte immunitarie adattative diventano più deboli, riducendo la protezione offerta.
La ricerca suggerisce tuttavia che questo processo non sia del tutto irreversibile: interventi mirati hanno dimostrato di poter migliorare la risposta immunitaria, offrendo nuove strade per preservare l’healthspan.
Inflammaging
Rappresenta il punto di convergenza sistemico di tutti i danni cellulari descritti finora: una condizione di attivazione pro-infiammatoria cronica, sistemica e di basso grado, che si instaura silenziosamente, in assenza di infezioni evidenti.
Non è l’infiammazione acuta che conosciamo come risposta a una ferita: è un rumore di fondo persistente che logora lentamente organi e tessuti.
Si sviluppa quando l’organismo rimane esposto per lunghi periodi a stimoli che attivano il sistema immunitario in modo continuo ma non acuto ed é caratterizzato da elevati livelli circolanti di citochine come IL-6 e TNF-α (Li et al., 2023).
Alla base ritroviamo sempre gli stessi protagonisti: cellule senescenti che si accumulano, un SASP che mantiene acceso il segnale infiammatorio e un sistema immunitario che non riesce più a contenerne gli effetti.
L’inflammaging è cruciale per l’healthspan!
Livelli persistentemente elevati di infiammazione in organi come midollo osseo, fegato e polmoni portano a danni d’organo progressivi e difficilmente reversibili.
In sintesi, l’inflammaging trasforma i micro-guasti cellulari in un declino visibile dell’intero organismo, riducendo la capacità di recuperare dagli stress quotidiani.
Non a caso, molti degli interventi più studiati nella ricerca sulla longevità, dai senolitici alla modulazione del SASP, mirano a ridurre questo stato infiammatorio cronico, nella prospettiva di preservare l’healthspan.
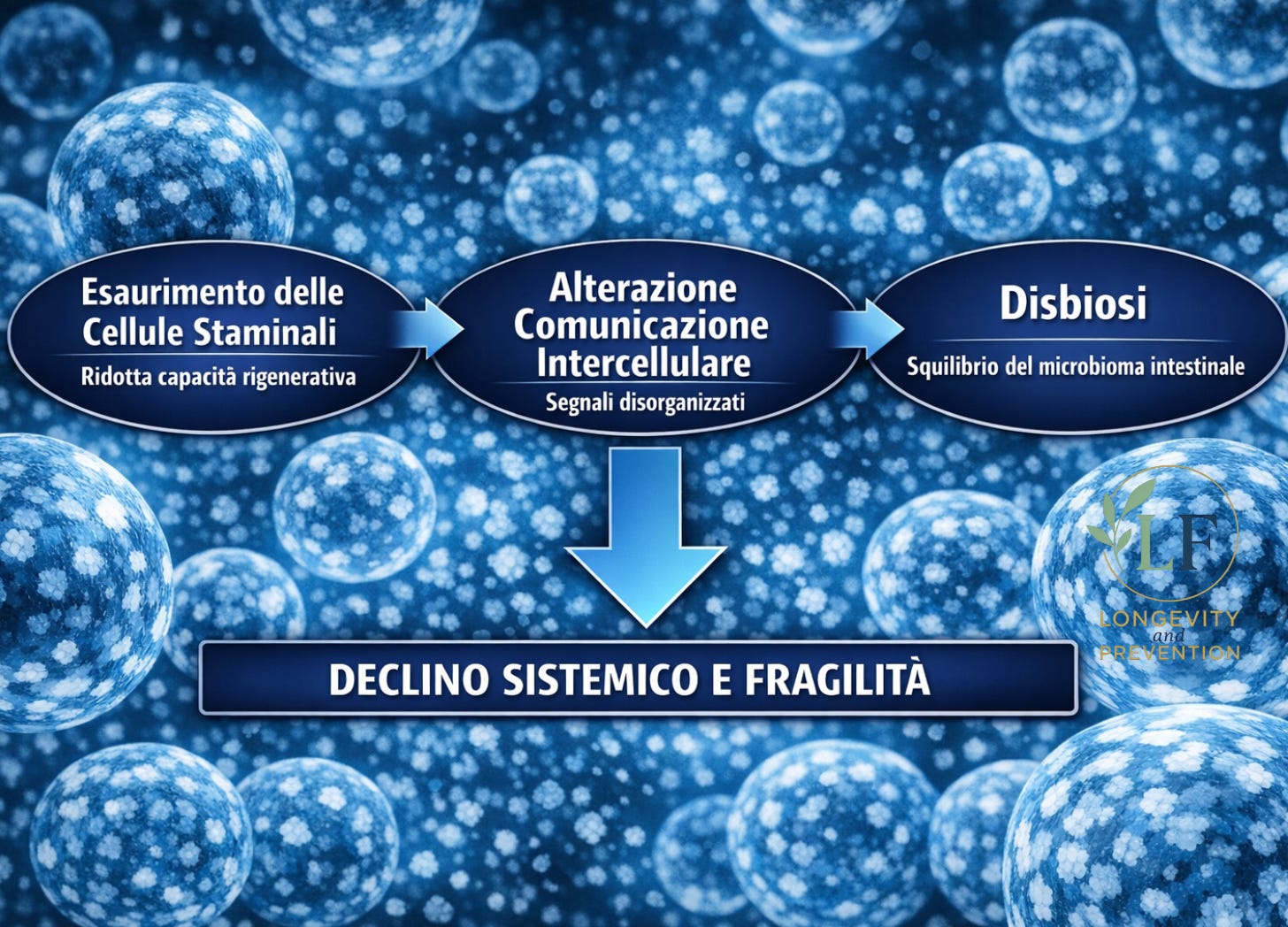
Declino sistemico: cellule staminali, comunicazione intercellulare e disbiosi
Quando i meccanismi di controllo non riescono più a far fronte al danno, il declino da cellulare si estende a tutto l’organismo con ripercussioni sulla vita quotidiana.
L’esaurimento delle cellule staminali, l’alterazione della comunicazione tra le cellule e la disbiosi sono i tre processi che segnano l’ingresso in questa fase e i primi ambiti sui quali è possibile intervenire.
Cellule staminali
Le cellule staminali adulte sono indispensabili per il mantenimento dell’omeostasi e la riparazione dei tessuti.
Con l’età queste cellule diminuiscono di numero, perdono il loro potenziale rigenerativo e la capacità di generare cellule differenziate, portando a un deterioramento della salute degli organi.
L’inflammaging contribuisce ulteriormente a questo processo, alterando i segnali che regolano l’attività rigenerativa delle cellule staminali.
La conseguenza è una crescente vulnerabilità: i tessuti recuperano più lentamente, sono più esposti allo stress e più inclini ad accumulare cellule danneggiate o senescenti.
Comunicazione intercellulare
In questa fase, i danni molecolari accumulati nelle singole cellule si manifestano a livello sistemico, modificando il modo in cui i vari organi dialogano tra loro.
Mentre i processi descritti sino ad ora riguardano principalmente ciò che accade all’interno delle cellule, l’alterazione della comunicazione intercellulare descrive come il “clima” generale dell’ organismo diventi disorganizzato con l’avanzare dell’età.
Il SASP contribuisce direttamente a questo deterioramento, diffondendo segnali infiammatori che alterano il comportamento delle cellule sane circostanti.
Questa alterazione del dialogo è uno dei meccanismi che genera la fragilità sistemica.
Disbiosi
Il microbioma intestinale è uno dei principali regolatori dell’equilibrio fisiologico: non è solo un insieme di batteri, ma una centrale biochimica che modula lo sviluppo e la funzione delle cellule immunitarie, il metabolismo e contribuisce alla protezione della barriera intestinale.
Con il passare degli anni si assiste a una perdita di batteri commensali protettivi a favore di una proliferazione di batteri potenzialmente dannosi che producono tossine dando origine al fenomeno della disbiosi oggi considerato un hallmark integrativo.
Dieta, farmaci e fragilità contribuiscono a rendere il microbiota meno resiliente.
Come evidenziato dalle ricerche, la disbiosi agisce sulle proteine che tengono sigillate le pareti intestinali generando alterazione della permeabilità intestinale: lo strato di muco protettivo si riduce, esponendo la parete intestinale a stimoli microbici che innescano risposte infiammatorie sistemiche.
Questa migrazione di tossine nel sangue è uno dei motori principali che alimentano l’infiammazione cronica in tutto l’organismo.
E’ confermata da numerose ricerche scientifiche l’esistenza di una relazione bidirezionale pericolosa: la disbiosi promuove la senescenza cellulare e l’infiammazione, le quali, a loro volta, alterano ulteriormente l’equilibrio del microbioma creando un ciclo che accelera il deterioramento non solo intestinale, ma di tutti gli organi vitali.
In sintesi, mantenere l’integrità della barriera intestinale e un microbioma diversificato non è solo una questione di digestione, ma una strategia fondamentale per preservare una comunicazione cellulare, ridurre l’inflammaging e migliorare la resilienza complessiva dell’organismo.
In conclusione
I dodici hallmark descritti mostrano come il declino biologico sia determinato da una rete interconnessa di meccanismi la cui alterazione si amplifica reciprocamente, traducendosi progressivamente in perdita di funzionalità e resilienza.
Comprendere queste dinamiche è il primo passo per riconoscere dove e come intervenire.
Nella Parte III vedremo come la ricerca stia trasformando questa conoscenza in strategie concrete per preservare e migliorare l’healthspan.
Se vuoi capire perché l’healthspan è diventato il parametro centrale della medicina moderna, trovi le basi nella Parte I disponibile qui.
Conoscere i meccanismi del declino è già, di per sé, un atto di prevenzione!
Riferimenti bibliografici essenziali
Wang, B., et al. (2024). The senescence-associated secretory phenotype and its physiological and pathological implications. Nature Reviews Molecular Cell Biology.
Li, X., et al. (2023). Inflammation and aging: signaling pathways and intervention therapies. Signal Transduction and Targeted Therapy.
López-Otín, C., et al. (2022). Hallmarks of Aging: An Expanding Universe. Cell.
McReynolds, M.R., et al. (2020). Age-related NAD+ decline. Experimental Gerontology.
Campisi, J., et al. (2019). From discoveries in ageing research to therapeutics for healthy ageing. Nature.
Dott. Letizia Foglieni – Medico Chirurgo – Divulgatrice scientifica – ideatrice di Longevity & Prevention
Se desideri restare aggiornato sui prossimi contenuti, puoi seguirmi su Substack. Se hai osservazioni o domande, sarò lieta di leggerle nei commenti.